がんゲノム医療について
理解が難しい『がんゲノム医療』
2017年春頃より、様々なメディアで『がんゲノム医療』という言葉が使われてきました。しかしこの言葉は、『がんのゲノム情報を使って行う医療行為・医療開発』という広い意味を持つため、理解が難しい言葉となってしまっています。その広い意味の中で、現状患者さんにとっての『がんゲノム医療』とは、『新しい検査を受けて、自分のがんに効果が期待できる薬がないかを探すこと』です。
自分に残された可能性を知る検査
がんゲノム検査では、がんの遺伝子情報を読み取り、がん細胞の性質をより詳細に解析します。その結果から、新たな治療の選択肢がないかを検索します。この薬剤を検索する段階では、以下の3点を考慮しません。
①該当薬剤が日本にあるかどうか。
②該当薬剤が日本で保険適用かどうか。
③該当薬剤の副作用が患者様にとって許容できると考えられるか。
つまり、治療費や副作用など、現実的に治療を行う際に問題となることは一度考えずに、まずは他の選択肢があるのかないのかを検索します。このため、薬剤が見つかったとしても、実際に治療を行うかに関しては慎重に判断しなければなりません
薬剤検索の根拠となる情報
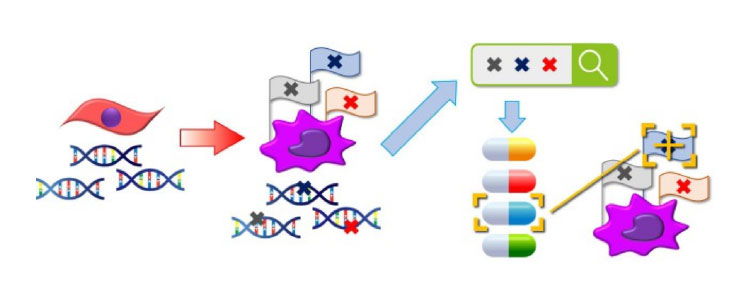
薬剤を探す際に、対応薬剤の根拠として用いる情報が、がん細胞の遺伝子の情報です。がんとは、正常細胞の設計図である遺伝子に異常が起きて、生じる疾患です。このがんという疾患の根底にある異常を詳細に解析することで、『詳細で正確な診断』を行うことが、がんゲノム医療の第一歩となります。その診断を元に、異常な設計図から出来上がった異常な目印を標的とした薬剤が存在しないか、報告されている全ての薬剤を検索にかけます。
がんゲノム医療は本当に効果があるのか?
がんゲノム医療において患者さんにとっての最も重要な疑問は、『がんのゲノム情報を基に選んだ薬剤は本当に効果があるのか?』という点です。この点に関しては、『現在調べている段階である』という解答が最も正しいと考えます。がんゲノム医療は、理論上は正しいと考えられますが、特に『がん種を問わずに効果があるのか』という点に関して、まだ正確な答えが得られていません。現在行われている多くの試験の結果を待つことが必要になります。このため、現状では標準治療を超えてお勧めするものではありません。この点に関しては、特に十分な理解が必要です。
SHIVA試験から学ぶこと
2012年から2014年にかけて、フランスでSHIVA試験と呼ばれる大規模な臨床試験が行われました※1。SHIVA試験は、がん種を問わずに、がんの分子生物学的な解析(ゲノム情報も含みます)に基づく分子標的治療と標準治療を比較した初めての臨床試験です。しかし残念ながら、結果は『有意差無し』でした。この結果から、がんゲノム医療に関して多くの議論が展開されましたが、最も注目された点の一つが、『薬剤選択の根拠の強さ』でした。
SHIVA試験では、少なくとも他のがん種では標準治療として用いられている薬剤から、まだ標準治療としてはどのがん種でも使用されていない薬剤まで、幅広い薬剤が使用されました。この点から、『薬剤選択の根拠の強さ』が統一されておらず、この『根拠の強さ』を重要視する意見が出てきました。
※1 Lancet Oncol, 2015. 16(13): p.1324-34.
米国におけるがんゲノム医療
米国では、2015年1月20日にアメリカのオバマ大統領が一般教書演説で、プレジション・メディシン(Precision Medicine)という医療・医学研究推進の政策を発表しました。プレジション・メディシンは、日本語では、『精密医療』と訳されることが多い言葉です。がんゲノム医療のように、より精密な診断を行うことで、研究を進めていく方針です。この発表後、多額の研究費ががんゲノム医療に投下され、研究が加速しています。現在では、多くの研究機関、ベンチャー企業が、がんゲノム検査を提供しています。
このような状況のため、米国ではがんゲノム情報を基にした治療が一部医療機関で既に行われています。2018年には、米国ユタ州の州都ソルトレイクシティにある施設から、がんゲノム情報を基にした治療を行った患者22例の解析で実際に予後が改善したとの報告も出ています※2。この報告は症例数も少なく、この一報だけでがんゲノム医療の有用性を結論付けることはできませんが、理論上正しいと考えられるがんゲノム医療の有用性を示した、非常に勇気づけられる結果です。
※2 Oncotarget, 2018. 9(15): p. 12316-12322.
日本におけるがんゲノム医療
日本でも、2019年より保険適用のがんゲノム検査が開始となりました。横浜市立大学附属病院では、この保険適用検査の開始に先駆けて、2016年11月より、自費診療としてMSK-IMPACTと呼ばれるがんゲノム検査を導入しました。MSK-IMPACTは、米国ニューヨークのメモリアルスロンケタリングがんセンターで開発された、がんゲノム検査です。
がんゲノム検査、MSK-IMPACT
横浜市立大学附属病院で提供しているがんゲノム検査は、2020年2月の段階では保険適用のがんゲノム検査とMSK-IMPACTです。今後、提供できる検査は増えていく可能性があります。ここでは、現在運用している検査のの特徴をまとめます。
初めてのFDA承認がんゲノム検査
米国食品医薬品局(FDA)は、2017年11月15日にMSK-IMPACTを腫瘍の遺伝子変化を解析する検査として初めて承認しました。MSK-IMPACTの質を保証するものです(参考ページはこちら)。
世界最大規模の解析遺伝子数
がんゲノム検査には、解析遺伝子数を絞り、費用を安くしたものと、解析遺伝子数を出来る限り多くとったものがあります。MSK-IMPACTは世界最大規模の解析遺伝子数を誇ります。経営母体がNPO法人であることから、値段も安く設定してあります。
融合遺伝子を検出可能
解析遺伝子数を絞っている検査の中には、融合遺伝子と呼ばれる遺伝子の変化を検査対象としないものもあります。分子標的薬の中には融合遺伝子を対象としたものもあることから、MSK-IMPACTは融合遺伝子も検査対象に含みます。
免疫チェックポイント阻害剤に対する効果予測因子を解析可能
免疫チェックポイント阻害剤と呼ばれる薬剤には、よく知られている効果予測因子が2種類あります。MSK-IMPACTでは、その2つとも解析可能です。
独自のデータベースを持ち、薬剤に対する『推奨の強さ』を提示可能
前述したように、がんゲノム医療において、『薬剤選択の根拠の強さ』は非常に大切な要素です。MSK-IMPACTでは、独自のデータベースから、下の4段階に『薬剤選択の根拠の強さ』を分類しています。これをエビデンスレベルと呼びます。

既に2万人の患者が同じ検査を受けている
MSK-IMPACTは、既に2万人以上の解析を行っています。これらの結果は、独自のデータベースに登録され、最初の1万人に関してはデータが公開されています。このデータは、臨床検査として行われたもののため、これまでの研究目的に行われてきたデータベースにはほとんど見られない、希少がんが多く含まれていることが大きな特徴です。横浜市立大学附属病院がんゲノム診断科では、これらのデータと比較して、最終レポートを作成しています。
がんゲノム検査の課題と限界
がんゲノム検査は、保険診療であっても高額な検査です。更に、検査によって効果があると考えられる薬剤が見つかった場合でも、多くの場合、保険診療内で使用することができません。この費用の問題が今後の課題と言えます。
また、がんゲノム検査により新しい薬剤が見つかる可能性は10%~20%と言われており、この点が現時点での限界と言えます。この10%の可能性を高いと見るか、低いと見るかという点で、患者さん自身の考え方が重要になります。例えば、10%であれば多くの場合がっかりするだけなので検査を受けない、という考え方もあります。逆に、10%でも上乗せできるのであれば検査を受けたい、と考える方もいます。これらは個人の考え方の違いなので、患者さん自身に説明した上で、検査の同意を得ています。
