研究内容
DAMPsによる生体応答制御機構の解明
― Decoding “Dying Messages” Released from Damaged Cells ―
生体は、がんや組織障害、感染などのさまざまな危機的状況に直面した際、それらを感知し、適切に応答することで、元の恒常状態へと回復しようとする高度な制御機構を備えています。このような応答過程において炎症反応は重要な役割を果たしますが、その反応が過度あるいは慢性的に持続した場合、組織障害や疾患の進展につながることが知られています。しかし、自己の細胞や組織がダメージを受けた際に、どのような機構によって炎症が誘導されるのか、また、なぜ炎症が収束せず慢性化してしまうのかについては、依然として未解明な点が多く残されています。
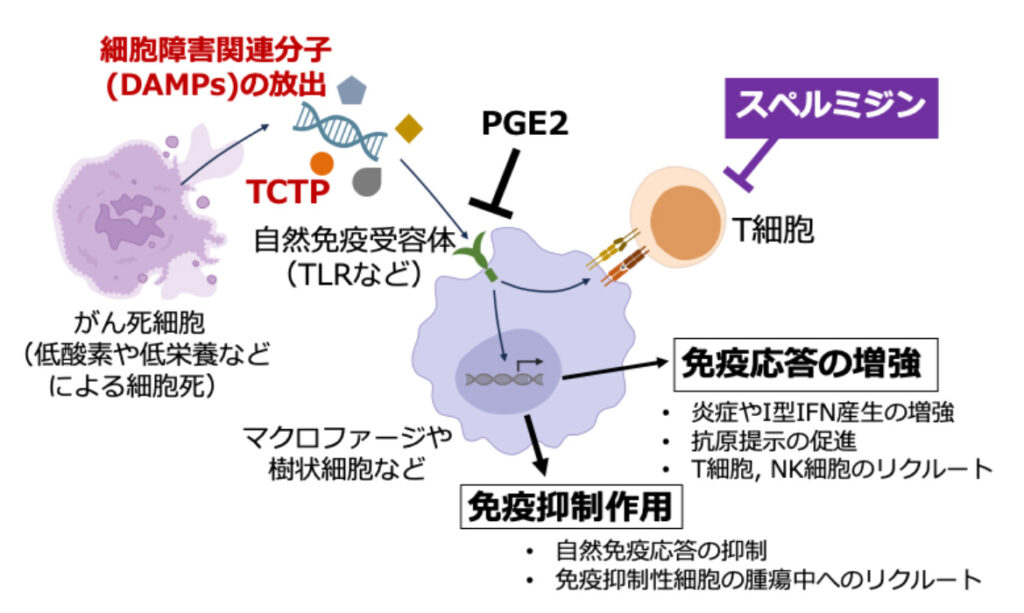
私たちは、ダメージを受けた細胞や死細胞から放出される内因性分子、いわゆる危機応答分子(Damage-associated molecular patterns;DAMPs、細胞障害関連分子やアラーミンとも呼ばれる)に着目し、これらの分子が生体応答や炎症制御に果たす役割の解明を進めています。これまでに、プロスタグランジンE2がDAMPsによる炎症誘導を抑制すること(PNAS, 113: 3844–3849, 2016)を明らかにするとともに、TLR2によって認識される新たな内因性分子としてTranslationally-controlled tumor protein(TCTP)を同定しました(Nat Immunol, 22: 947–957, 2021)(図1)。さらに、がん死細胞から放出されたポリアミンであるスペルミジンがT細胞の活性化を阻害し、抗腫瘍免疫応答を抑制することを見出しています(PNAS, 120: e2305245120, 2023)(図1)。加えて現在、生体の恒常性維持に関与する新たな分子群の同定にも取り組んでいます。分子生物学的手法や先端的オミクス解析を活用し、DAMPsの同定と機能解析を通じて、危機応答の制御機構を明らかにすることを目指しています。
腫瘍微小環境におけるDAMPsと腫瘍免疫・病態制御機構の解明
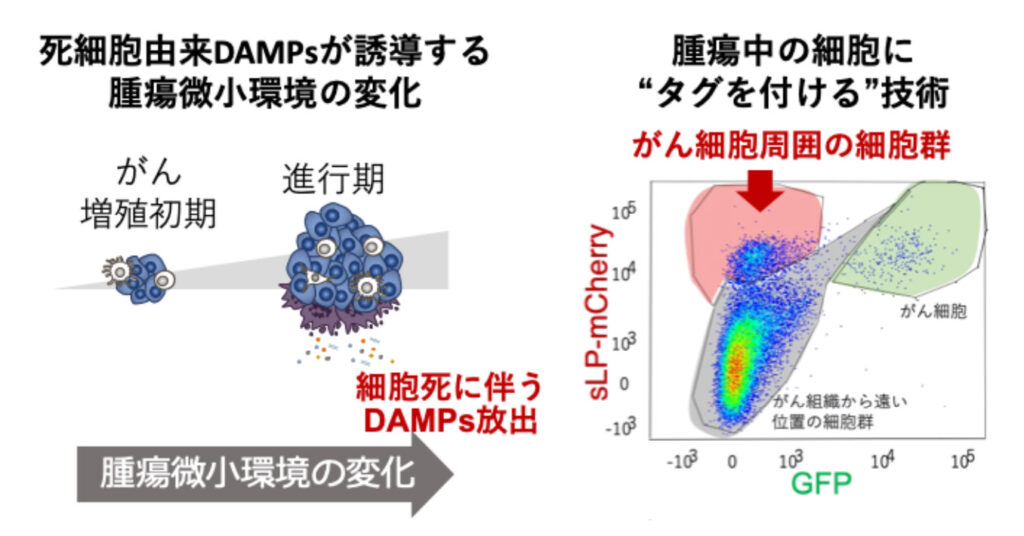
腫瘍の増殖過程や治療介入に伴い、腫瘍組織内にはダメージを受けた細胞や死細胞が多数生じます。これらの細胞からは、DAMPsをはじめとするさまざまな内因性分子や代謝産物が放出され、腫瘍微小環境における免疫細胞の活性化や抑制、細胞間相互作用の変化を通じて、病態形成に深く関与していると考えられています。私たちの研究から、死細胞由来分子には免疫応答を促進するものだけでなく、過剰な免疫反応を抑制し、応答の質や持続性を制御する分子も存在することが明らかになりつつあります。
現在は、腫瘍免疫微小環境という枠組みに加え、腫瘍局所におけるストレス応答や組織恒常性の破綻、さらには臓器・組織特異的な生体応答制御機構という視点から、死細胞由来分子の役割を多角的に解析しています。マウスモデルを用いた解析に加え、腫瘍微小環境を時空間的に標識・追跡する微小環境ラベル法を導入し(図2)、腫瘍の進展や治療介入に伴う微小環境の変遷を解析しています。さらに、これらの手法にオミクス解析を組み合わせることで、腫瘍組織ごとに異なる免疫応答制御ネットワークの理解を目指しています。これらの研究を通じて、腫瘍免疫の制御原理の解明とともに、新たな治療標的分子や免疫療法戦略の創出につなげることを目標としています。